Дистрофия
Общие сведения
Что такое дистрофия? Дистрофия (лат. Dystrophia) представляет собой патологический процесс, обусловленный количественными/качественными изменениями в метаболизме клеток тканей/межклеточном веществе, приводящие к их структурным изменениям. В обиходе часто можно встретить выражение «дистрофик» или ты можешь стать дистрофиком применительно к очень худому человеку, то есть, это мужчины или женщины с крайней степенью истощения организма. Непосредственной причиной дистрофий являются различного рода нарушения клеточных/внеклеточных механизмов, обеспечивающих трофику тканей. Изучением дистрофических процессов занимается такая область медицинских знаний, как патологическая анатомия человека, изучающая морфологические/структурные изменения в тканях организма, возникающие в результате воздействия экзогенных/эндогенных факторов и их влияние на развитие болезнетворного процесса.
В основе дистрофии могут лежать различные внутриклеточные/внеклеточные процессы аккумуляции/уменьшения различных веществ: жидкости, белков, жиров, липидов, углеводов; пигментов; образование аномальных веществ (например, продуктов нарушенного метаболизма); процессы распада различного рода структур. Дистрофические процессы могут протекать в тканях различных органов, формируя ту или иную патологию, например:
- В структурах глаза — дистрофия макулярной области сетчатки (дистрофия Штаргардта) или периферическая витреохориоретинальная дистрофия, затрагивающая сетчатку, стекловидное тело и хориоидею (сосудистую оболочку) глаза. Периферическая витреохориоретинальная дистрофия сопровождается высоким риском отслойки сетчатки.
- Нервной системы — болезнь Фридрейха (син. атаксия Фридрейха), сопровождающаяся нарушением чувствительности и мышечной атрофией.
- Мышечной ткани, например, миотоническая дистрофия, которая проявляется нарушением способности мышц к расслаблению (релаксации) после их сокращения. Миотоническая дистрофия затрагивает процессы развития/функционирование скелетной/гладкой мышечной ткани разных тканей и органов.
При этом, они могут протекать преимущественно в паренхиме, строме или одновременно в паренхиме и строме, в соответствии с чем выделяют определенные виды дистрофий.
Паренхиматозные дистрофии
Для этого вида дистрофий характерно нарушения обмена в паренхиматозных органах (почки, сердце, печень). В основе паренхиматозных дистрофий лежит недостаточность конкретного ферментативного механизма (ферментопатии приобретенного/наследственного генеза), необходимого для выполнения специфических функций клеток (кардиомиоцитов гепатоцитов, нефроцитов). Паренхиматозные дистрофии включают:
паренхиматозные диспротеинозы (син. белковая дистрофия), сопровождающиеся появлением включений белковой природы в цитоплазму клеток, гидратацией клетки в них накоплением ионов натрия. Морфологически это гиалиново-капельная дистрофия, гидропическая дистрофия, роговая и зернистая дистрофия.
Гиалиново-капельная дистрофия характеризуется появлением в цитоплазме клетки гиалиноподобных крупных включений белка и всегда приводит к смерти клетки в то время, как при гидропической дистрофии в клеточной цитоплазме появляются вакуоли (син. вакуольная дистрофия), которая зачастую завершается развитием баллонной дистрофии с последующей смертью клетки в результате колликвационного некроза. Развивается в почках при нефротическом синдроме, гломерулонефрите, амилоидозе (дистрофия эпителия канальцев); в печени при вирусном, алкогольном гепатите, холестазе, билиарном циррозе (дистрофия в гепатоцитах) и значительно реже встречаются в сердечной мышце.
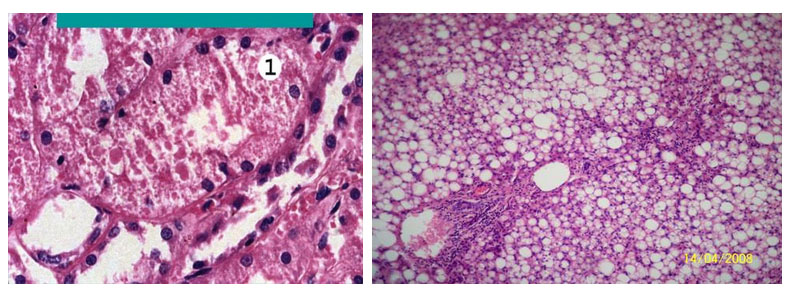
Гиалиново-капельная дистрофия и гидропическая (вакуольная) дистрофия
Зернистая дистрофия, наоборот, относится к поверхностной и в большинстве случаев при устранении причины является обратимой дистрофией, однако, при продолжающемся патологическом действии процесс может стать необратимым, преобразуясь в некроз. Органы при ней становятся немного набухшими, а при разрезе поверхность выглядит мутной и тусклой. Ее развитию способствуют различного рода инфекции и интоксикации. Развивается чаще в почках (зернистая дистрофия эпителия извитых канальцев почки), реже в печени, вызывая дискомплексацию печеночных балок и в сердечной мышце и этом, дистрофия сердечной мышцы сильно не выражена (фото ниже).
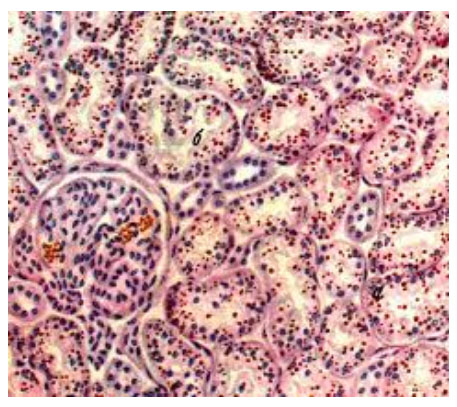 Роговая дистрофия (син. патологическое ороговение). Для нее характерно избыточная выработка в ороговевающем эпителии рогового вещества, что проявляется такими заболеваниями как (ихтиоз/гиперкератоз) или его там, где его в норме не должно быть (лейкоплакия, патологическое ороговение слизистых — гиперкератоз). При этом, патологический может быть распространенным или локализованным. Основными причинами развития роговой дистрофии являются вирусные инфекции, хроническое воспаление, нарушение развития кожи, авитаминозы. Исходом этого вида дистрофии в начале процесса может быть восстановление ткани при устранении причины, а в запущенных случаях клети погибают (фото ниже).
Роговая дистрофия (син. патологическое ороговение). Для нее характерно избыточная выработка в ороговевающем эпителии рогового вещества, что проявляется такими заболеваниями как (ихтиоз/гиперкератоз) или его там, где его в норме не должно быть (лейкоплакия, патологическое ороговение слизистых — гиперкератоз). При этом, патологический может быть распространенным или локализованным. Основными причинами развития роговой дистрофии являются вирусные инфекции, хроническое воспаление, нарушение развития кожи, авитаминозы. Исходом этого вида дистрофии в начале процесса может быть восстановление ткани при устранении причины, а в запущенных случаях клети погибают (фото ниже).
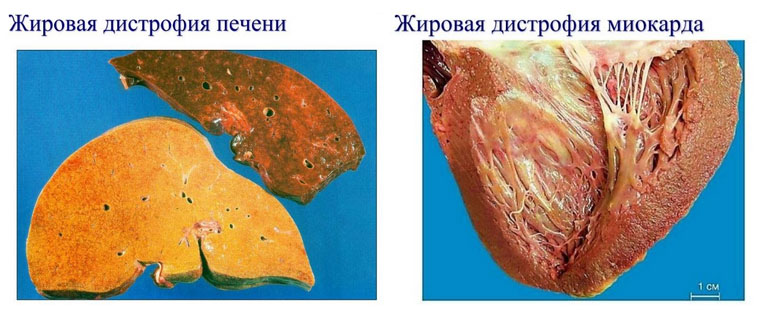
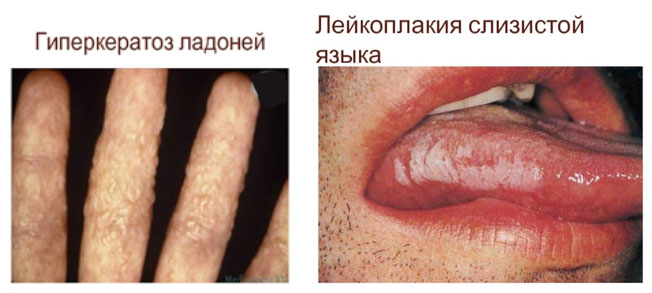 Паренхиматозные липидозы (син. жировая дистрофия). Для них характерно нарушения жирового обмена в цитоплазме вследствие дисбаланса между процессами поступления/утилизации и выведением липидов в гепатоцитах, что проявляется накоплением капель триглицеридов в цитоплазме клеток. Жировая дистрофия развивается чаще в печени, почках, миокарде и проявляется жировой дистрофией печени при общем ожирении, сахарном диабете, алкоголизме, анемии, гипоксии, недостатке в пище белка, заболеваниях ЖКТ, действии токсичных веществ (фосфор, этанол, углерод). Жировая дистрофия печени в большинстве случаев обратима, однако при присоединении некроза, возможно, развития печеночной недостаточности. Жировая дистрофия миокарда развивается преимущественно на фоне гипоксии (ХСН, анемии), интоксикаций (отравление мышьяком/фосфором, дифтерийная, алкогольная дистрофия).
Паренхиматозные липидозы (син. жировая дистрофия). Для них характерно нарушения жирового обмена в цитоплазме вследствие дисбаланса между процессами поступления/утилизации и выведением липидов в гепатоцитах, что проявляется накоплением капель триглицеридов в цитоплазме клеток. Жировая дистрофия развивается чаще в печени, почках, миокарде и проявляется жировой дистрофией печени при общем ожирении, сахарном диабете, алкоголизме, анемии, гипоксии, недостатке в пище белка, заболеваниях ЖКТ, действии токсичных веществ (фосфор, этанол, углерод). Жировая дистрофия печени в большинстве случаев обратима, однако при присоединении некроза, возможно, развития печеночной недостаточности. Жировая дистрофия миокарда развивается преимущественно на фоне гипоксии (ХСН, анемии), интоксикаций (отравление мышьяком/фосфором, дифтерийная, алкогольная дистрофия).
Углеводные дистрофии. Для этого вида дистрофий характерно нарушением обмена гликогена/гликопротеидов. К углеводным паренхиматозным дистрофиям, обусловленных нарушением процесса обмена гликогена относятся сахарный диабет и гликогенозы (наследственные углеводные дистрофии).
Развивающаяся абсолютная/относительная недостаточность инсулина при сахарном диабете вызывает нарушение утилизация глюкозы и процесса синтез гликогена, что приводит к повышается в крови содержания глюкозы и ее появлению в моче на фоне истощения запасов гликогена в мышцах/печени. Поражаются почечные канальцы, а также клубочки, у которых базальная мембрана становится более проницаемой для белков плазмы/сахаров. Нарушение процесса синтеза гликогена в печени способствует ее инфильтрации жирами с постепенным развитием жировой дистрофии печени.
Гликогенозы развиваются при наследственных заболеваниях (болезни накопления, ферментопатии) и обусловлены нарушениями обмена гликогена. Избыточное накопление гликогена отмечается преимущественно в скелетных мышцах, клетках миокарда, печени/почках, что вызывает вторичное повреждение клетки и некроз.
Паренхиматозные углеводные дистрофии, обусловленные нарушением обмена гликопротеидов, проявляются накоплением в клетках мукоидов/муцинов (слизистых веществ), поэтому зачастую ее называют слизистой дистрофией. Усиленное образование/изменение физико-химических свойств слизи приводит к гибели клеток.
Примером может быть слизистая дистрофия при муковисцидозе, характеризующегося изменением качества слизи (высокая вязкость, густая, тяжело выводится), что способствует развитию ретенционных кист/склероза (кистозный фиброз).
Стромально-сосудистые дистрофии (син. мезенхимальные дистрофии). Дистрофии такого рода обусловлены нарушениями обмена веществ непосредственно в интерстициальной соединительной ткани, состоящей из эластина, белков коллагена и гликозаминогликанов, формирующих строму органов/стенок сосудов. Для этой группе дистрофий характерно накопление в соединительной ткани различных продуктов метаболизма, что способствует развитию патологических состояний. Стромально-сосудистые дистрофии также подразделяют на белковые, жировые и углеводные.
Стромально-сосудистые диспротеинозы. В группе диспротеинозов выделяют:
- Мукоидное набухание. Проявляется преимущественно процессами декомпозиции (распадом связи аминогликанов и белков, при которых происходят неглубокие поверхностные изменения структуры соединительной ткани). Основное вещество незначительно набухает и изменяет присущие ему физико-химические свойства. Внешне органы не изменены, функция страдает незначительно. Процесс обратимый. К факторам, способствующим его развитию, относятся иммунные нарушения (эндокринные нарушения/ревматическая болезнь, инфекционные заболевания, гипоксии (атеросклероз, гипертоническая болезнь), инфекционно-аллергические заболевания.
- Фибриноидное набухание. Представляет собой необратимую дезорганизацию соединительной ткани, обусловленную деструкцией волокон и ткани, сопровождающееся образованием фибриноида и существенным повышением сосудистой проницаемости. Процесс необратим. Его исходом являются склероз, некроз, гиалиноз.
- Гиалиновая дистрофия. Является исход разных патологических процессов: фибриноидного набухания, воспаления, склероза, плазматического пропитывания, некроза. Различают гиалиноз сосудов и собственно соединительной ткани. Может быть как системным, так и местным (фиброзные спайки серозных полостей, рубцы, склероз сосудов). В большинстве случаев исход неблагоприятный, реже наблюдается рассасывание гиалиновых масс.
- Амилоидоз – вид белковой дистрофии, развивающейся в качестве осложнений различных инфекционно-воспалительных заболеваний или опухолей.
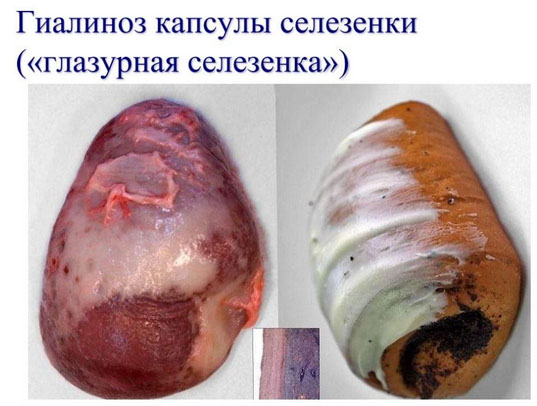
Мезенхимальные липидозы
Жировые мезенхимальные дистрофии развиваются на фоне нарушений обмена нейтрального жира/холестерина. Нейтральный (запасный жир) в норме накапливается в жировых депо для обеспечения энергетических потребностей человеческого организма. В основе дистрофии этого типа избыточное накопление жира в тканях, где он в норме должен отсутствовать или уменьшение его количества. Общее увеличение нейтрального жира проявляется тучностью/общим ожирением. Основными причинами являются нейроэндокринные нарушения процесса регуляции жирового обмена, возникающие на фоне поражения гипофиза, заболеваний ЦНС, избыточного питания (алиментарное ожирение). К тяжёлым правлениям относится ожирение сердца, когда жир откладывается между мышечными волокнами/под эпикардом, что приводит к атрофии миокарда и резкому снижению его функции. Нарушение холестеринового обмена приводит к его очаговым накоплениям в интиме крупных кровеносных сосудов, что является основой развития атеросклероза (рис. ниже).
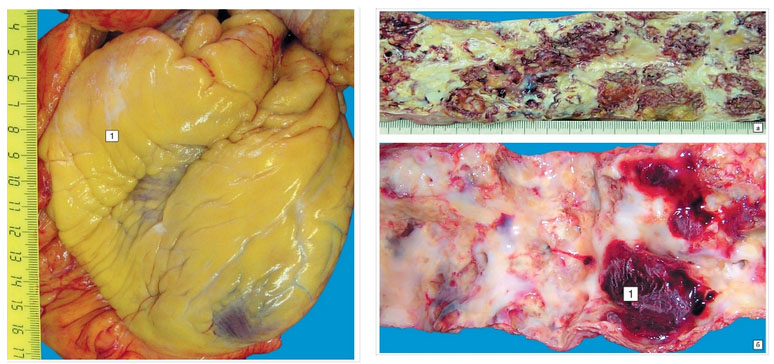
Ожирение сердца, атеросклероз аорты с липидными/атеросклеротическими изменениям
Мезенхимальные углеводные дистрофии. В их основе нарушение обмена гликопротеидов/гликозаминогликанов. Проявлением этого вида дистрофии является развитие густой слизеподобной массы на месте соединительной ткани и жировой клетчатки, что обусловлено высвобождением хромотропных веществ из связей с белками, которые накапливаются в межуточном веществе и постепенно происходит замещение коллагеновых волокон соединительной/жировая ткани, стромы органов на слизеподобную массу. Обусловлена нарушением эндокринных желёз (микседема, кахексия, болезни накопления).
Смешанные дистрофии
Смешанные дистрофии являются морфологическим проявлением расстройства метаболизма преимущественно сложных белков (нуклеопротеидов, эндогенных пигментов-хромопротеидов, а также липопротеидов и минералов как в паренхиме, происходящие так и в стенках сосудов/строме органов и тканей). Наиболее часто манифестируют различными нарушениями эндогенных пигментов (хромопротеидов), то есть, синтезируемых непосредственно в организме и придающих тканям/органам различную окраску (гемоглобин, ферритин, гемосидерин, гематоидин, гемин, порфирины и др.). На практике проявляются такими нарушениями как:
- общий/локальный гемосидероз, развивающийся в очагах кровоизлияний, при заболеваниях системы кроветворения, отравлениях гемолитическими ядами, некоторых инфекциях (малярия, сепсис, возвратный тиф, бруцеллез), при переливании крови другой группы, резус-конфликте.
- гемохроматоз, развивающийся при нарушении всасывания пищевого железа в ЖКТ, проявлением которого является бронзовая окраска кожи/пигментный цирроз печени;
- желтуха (гемолитическая, механическая, печеночная) — обусловленная избыточным накоплением билирубина в плазме крови, манифестирует желтушным окрашиванием кожи, слизистых/серозных оболочек, склер, внутренних органов;
- порфирии, обусловленные накоплением в тканях, крови, моче предшественников порфирина, проявляются появлением на коже дерматита, эритем, рубцов, изъязвлений, которые впоследствии переходят в депигментированные участки, при этом развивается светобоязнь/повышается чувствительность к ультрафиолету.
Существует и множество других видов расстройств (гипермеланоз, невис, меланома, липофусциноз и др.), однако они не являются темой этой статьи.
Патогенез
Среди патогенетических механизмов лежащих в основе дистрофических изменений выделяют:
- Инфильтрацию — проникновение продуктов обмена из лимфы/крови в клетки/межклеточное пространство в избыточном количестве и их последующее накопление, обусловленное недостаточностью ферментных систем, необходимых для метаболизма этих продуктов (белковая инфильтрация эпителия проксимальных канальцев почек, встречающаяся при нефротическом синдроме или, например, инфильтрация липопротеидами/холестерином крупных артерии/аорты при атеросклерозе).
- Фанероз (декомпозиция) — распад межклеточного вещества/клеточных структур, приводящие к нарушению клеточного (тканевого) обмена веществ и накоплению продуктов нарушенного метаболизма в клетке (например, фибриноидное набухание соединительной ткани, характерное для ревматических заболеваний, жировая дистрофия мышечных клеток миокарда при интоксикации).
- Извращенный синтез — образование в клетках/тканях веществ, которые в норме для них неприсущие (выработка в клетке аномального белка амилоида/аномальных белково-полисахаридных амилоидных комплексов в межклеточном пространстве; синтез в эпителии нефрона гликогена при сахарном диабете).
- Трансформацию — образование из общих исходных продуктов продукции одного вида обмена, идущие на синтез белков, жиров, углеводов (например, трансформация жиров/углеводов в белки, усиленная трансформация глюкозы в гликоген).
Установлено, что основными морфогенетическими механизмами дистрофий являются инфильтрация, фанероз и зачастую они относятся к различным стадиям развития патологического процесса. Но в некоторых тканях/органах в силу их структурно-функциональной специфики преобладает один из вышеописанных морфогенетических механизмов.
Классификация
В основу классификации дистрофий положены различные признаки, на основании которых принято выделять различные виды дистрофии:
- По локализации морфологических изменений — паренхиматозные, мезенхимальные (стромально-сосудистые) и смешанные.
- По преобладающему нарушению метаболизма (белковые, углеводные, жировые, минеральные).
- По происхождению (приобретенные, наследственные).
- По распространенности патологического процесса (общие и местные).
Причины
Дистрофии относятся к полиэтиологическим патологическим процессам. Каждый вид дистрофии имеет свои причины развития. При этом, причины, способные потенциально вызывать дистрофию, могут действовать непосредственно или через рефлекторные/гуморальные механизмы, то есть, опосредованно. Степень/характер повреждения определяется природой/длительностью действия и силой повреждающего фактора, особенностями структуры/функции ткани или органа и реактивностью организма. Соответственно, при некоторых видах дистрофий возникают обратимые поверхностные изменения, при других — необратимые глубокие, сопровождающиеся высоким риском гибели клеток/тканей, а зачастую и целых органов. Причины развития дистрофий чрезвычайно разнообразны, среди которых можно выделить основные:
- Разнообразные факторы, повреждающие процесс ауторегуляции клетки. К ним относятся токсические вещества различного генеза, в том числе токсины, продуцируемые микроорганизмами; физические/химические агенты в виде низкой/высокой температуры, ионизирующая радиация, химические вещества (соли тяжелых металлов, органические вещества, щелочи/кислоты).
- Ферментопатии (энзимопатии) разного генеза (наследственные, передаваемые по аутосомному рецессивному/доминантному типу и приобретенные).
- Цитопатогенные вирусы. Вызывают лизис клетки различным путем (прямым включением в клеточные мембраны/встраивание в клеточный геном, путем индицирования иммунного ответа).
- Длительно/тяжело протекающие инфекции (туберкулез, дифтерия, сепсис).
- Острые/хронические интоксикации (алкоголь, фосфор, хлороформ, мышьяк), приводящие к нарушениям обмена.
- Ревматические болезни (ревматоидный артрит, ревматизм, узелковый периартериит, системная красная волчанка/склеродермия).
- Алиментарная недостаточность/несбалансированное питание, авитаминозы, сопровождающееся дефицитом белков, жиров и ферментов.
- Функциональные нарушения транспортных/энергетических систем, лежащих в основе поддержания клеточного метаболизма и сохранности структуры клеток тканей (гипогликемия, приводящая к недопроизводству молекул АТФ; гипоксия, развивающаяся в результате обструкции дыхательных путей, ишемии, анемии, нарушении структуры гемоглобина, приводящие к снижению транспортировки кровью кислорода).
- Расстройства нервной/эндокринной регуляции в виде болезней эндокринных органов (гиперпаратиреоз/тиреотоксикоз, диабет); болезни нервной системы (опухоли головного мозга, нарушенная иннервация).
Те или иные повреждающие факторы, воздействуя непосредственно на биохимические процессы межклеточных структур/клетки способствуют как морфологическим изменениям, так и функциональным нарушениям. При этом, точный момент, при котором дистрофические процессы становятся необратимыми остается до настоящего времени неизвестным.
Симптомы
Поскольку дистрофия, как патологический процесс является составляющим элементом патогенеза большого числа заболеваний рассмотреть их симптоматику в короткой статье не представляется возможным. В качестве примера, рассмотрим лишь болезнь Фридриха и миотоническую дистрофию.
Наследственная атаксия Фридрейха
Атаксия Фридрейха (АФ) относится к врожденным заболеваниям, передаваемых по аутосомно-рецессивному типу то есть, дети с этой патологией рождаются у пары клинически здоровых родителей, но которые являются носителями гена, вызывающего патологию. Наиболее часто встречаемая врожденная атаксия: показатель встречаемости варьирует в пределах около 2-7 случаев/100 тысяч человек. При АФ поражаются:
- нейроны центральной/периферической нервной системы: пучки Голля, Бурдаха, Говерса, Флексига, кора головного мозга, клетки коры мозжечка, пирамидные пути, задние корешки, спинномозговые ганглии, периферические нервы, базальные ганглии, а также проводящие пути спинного мозга;
- клетки миокарда;
- поджелудочная железа: β — клетки островков Лангерганца;
- клетки сетчатки глаза;
- клетки костной ткани.
Протекает на фоне прогрессирующей дегенерации ЦНС и периферической нервной системы. Симптоматика заболевания появляются преимущественно на 1-2 десятилетии жизни, реже — позже. Основными признаками являются пошатывание/неуверенность, спотыкание и частые падения во время ходьбы, слабость в ногах, тремор, дизартрия, нарушения слуха. Постепенно исчезают надкостничные/сухожильные рефлексы (ахилловы/коленные). Зачастую ранним проявлением является ревмокардит, нистагм, расстройства сидения. При физикальном обследовании пациенты не могут выполнить пяточно-коленную пробу, отмечается выраженное покачивание в позе Ромберга, усиливающееся при закрывании глаз.
Постепенно нарастает нарушение глубокой чувствительности, прогрессирует мышечная атрофия, которая первоначально превалирует на нижних конечностях, а позже распространяется и на верхние конечности. Быстро формируется тотальная арефлексия, развивается катаракта и атрофируется зрительный нерв, что приводит к слепоте, деменции, нарушению функция тазовых органов. Практически параллельно развиваются эндокринные нарушения в виде дисфункции яичников, гипогонадизма, сахарного диабета. Появляются кардиомиопатии и различного рода деформации скелета: кифосколиоз, искривление позвоночника, «стопа Фридрейха», косолапость, деформация пальцев рук/ног. Болезнь неуклонно прогрессирует, в случаях отсутствии своевременного/адекватного лечения, длительность болезни не превышает 20 лет, реже пациенты доживают до 70-80 лет. Непосредственной причиной смерти являются инфекционные осложнения и сердечно-легочная недостаточность.
Миотоническая дистрофия
Клинические проявления МД манифестируют мышечной (миотония, миопатия, миалгия) и вне мышечной симптоматикой в виде с вегетативно-трофических нарушений. При этом, проявления заболевания несколько отличаются в зависимости от типа (1 и 2 тип). В основе заболевания мутации на длинном плече хромосом в различных генах. Тип 1 протекает более тяжело, чем тип 2.
Начало заболевания существенно варьирующим: от периода пренатальности до 50-60 лет. По возрасту начала заболевания выделяют 4 формы: врожденная (манифестирует сразу после рождения ребенка), юношеская (дебют заболевания в период от года до13-15 лет), классическая форма (20-30 лет) и минимальная форма, проявляющаяся в 50-60 лет. Кроме различия в возрасте манифестации проявления заболевания также имеются различия в симптоматике этого заболевания в зависимости от формы. К общим признакам заболевания относятся:
миотонический/миопатический синдромы. Характерно поражение мышц дистальных отделов верхних/нижних конечностей, лица, дыхательной мускулатуры, что выражается миотоническими спазмами в мышцах-сгибателях рук/ног, преимущественно в пальцах, а также жевательных мышцах, что проявляется проявляются неспособностью мышц к расслаблению (релаксации) после их сокращения при попытке открыть рот, разжать кулак, свистнуть.
На поздних стадиях заболевания проявления активной миотонии исчезают по мере нарастания мышечной слабости/атрофии. Появляется слабость и симметричные мышечные подергивания, атрофия выражены преимущественно в височных, жевательных, надостных, грудинно-сосцевидных мышцах, реже наблюдается атрофии круговой мышцы глаза, мимических мышц, вследствие чего лицо приобретает угрюмо-печальное маскообразное выражение. При поражении бульбарных мышц изменяется оттенок голоса, речь делается монотонной/малоразборчивой, возникает поперхивание, затруднение глотания. Миотонические спазмы дыхательных мышц и их слабость способствуют ограничению движений грудной клетки и нарушению вдоха/выдоха, что снижает легочную вентиляцию, изменяет частоту, ритм и амплитуду дыхания.
Из вне мышечной симптоматики характерно нарушение функции ЦНС, что проявляется сонливостью, постоянной усталостью, апатией. Часто выявляется снижение интеллекта/задержка психического развития. Наиболее частыми являются симптомы со стороны сердца (кардиомиопатия, аритмии, застойная сердечная недостаточность, атриовентрикулярные блокады). Из респираторной симптоматики — гиповентиляции, апноэ во время сна и аспирационная пневмония. Часто поражаются глаза (двусторонняя миотоническая катаракта). Характерны эндокринные расстройства (нарушение менструального цикла, гипогонадизм у мужчин, нарушения репродуктивной функции, сахарный диабет 2-го типа). Могут иметь место нарушение функции поджелудочной/щитовидной железы, половых желез, гипоталамуса.
Одним из частых проявлений является облысение в лобно-теменной области. Облысение сочетается с изменением структуры волос. Волосы становятся ломкими, тусклыми на фоне повышенной ломкости/тусклости волос. Зачастую страдает функция ЖКТ (дисфагии/нарушения перистальтики), отмечается прогрессирующий сколиоз, появляются костные деформации лобных костей, грудной клетки, стоп.
У детей при врожденной форме миотонической дистрофии отмечается выраженная мышечная гипотония с поражением мимической, жевательной и глазодвигательных мышц (симптомокомплекс «вялого ребенка»).
Характерны трудности вскармливания из-за миотонических спазмов при сосательных движениях и акте глотания, респираторный дистресс-синдром, задержка темпов развития двигательных навыков, у многих детей — и олигофрения. Заболевание быстро прогрессирует, и часто приводит к внезапной смерти в раннем возрасте, но чаще при классической форме смерть наступает в 50-60 лет вследствие сердечных осложнений, пневмонии и других интеркуррентных заболеваний.
Анализы и диагностика
Для диагностики используются самые различные методы, начиная от молекулярной и генетической до различных инструментальных (УЗИ. МРТ, КТ, электрокардиоргамма/эхокардиография, электромиография, биопсия мышц и др.) и лабораторных методов исследования в зависимости от заболевания, протекающего с дистрофическими проявлениями.
Лечение
Лечение болезней, протекающих с явлениями дистрофии определяется конкретным заболеванием. Рассмотри лишь уже рассмотренные заболевания.
Лечение атаксии Фридрейха
Полного выздоровления не наступает, а основное лечение сводится к замедлению его прогрессирования и снижению риска развития ряда симптомов/осложнений. С этой целью показаны антиоксиданты, препараты митохондриального ряда и другие лекарственные средства, уменьшающие аккумуляцию в митохондриях железа и влияющие на различные уровни энергетического метаболизма. Рекомендуется назначение одновременно как трех и более лекарственных средств из этих групп: антиоксиданты — витамины А и Е, Глицин, Идебенон (синтетический аналог коэнзима Q 10), который эффективно тормозит развитие нейродегенеративного процесса, а также, развитие гипертрофической кардиомиопатии. Также назначаются кофакторы энзимных реакций и препараты, способствующие повышению активности митохондрий (Кокарбоксилаза, Нивалин, Прозерин, Оксазил, Нейромидин, Галантамин, Рибоксин, Предуктал, 5-гидроксипрофан).
Проводится общеукрепляющая терапия (витамины), а терапия, направленная на нормализацию тканевого метаболизма (Пирацетам, Тиоцетам, Церебролизин, Метионин, Аминалон, АТФ-лонг, Актовегин, Гинкго-билоба, Прозерин, Пиритинол, Никотиновая кислота) курсами. Для замедления дистрофических процессов могут назначаться глюкокортикоиды (Преднизолон, Оксазолон, Дефлазакорт). Показаны препараты с нейротрофическим эффектом (Церебрум композитум, Траумель).
Хороший эффект дает метаболическая терапия, улучшающая процессы метаболизма в клетках миокарда, костной ткани, печени, скелетных мышцах, способствующая нормализации жирового обмена (Левокарнитин, витамин Д3, препараты кальция, витамины группы В – Цианокобаламин/Тиамин-хлорид). Показано введение в спастичные мышцы Ботулотоксина. Дополнительно проводится лечение конкретно развившегося заболевания со стороны сердечно-сосудистой системы, диабета, катаракты, поджелудочной железы, искривлений позвоночного столба и др.
Лечение миотонической дистрофии
Какой-либо этиопатогенетической терапии миотонической дистрофии нет. Проводится преимущественно симптоматическое лечение, включающее в комплекс мероприятий при нервно-мышечных заболеваниях. Могут назначаться препараты, уменьшающие ригидность мышц (Мексилетин, Хинидин, Карбамазепин, Фенитоин, Прокаинамид и др.). Существенное облегчение приносит ортопедическая коррекция, физиотерапевтическое лечение. Для поддержания мышц назначается фармакопунктура с церебролизином, актовегином, нейромидином, цианокобаламином. При развитии остеопороза показаны кальцийсодержащие препараты, например, Кальцемин Адванс. При развитии конкретного заболевания проводится его лечение.
Доктора
Лекарства
- Препараты с «метаболическим» действием, улучшающие тканевой метаболизм (Элькар, витамин Е, А, Рибоксин, Метионин, АТФ-Лонг, Цитофлавин, Пирацетам, Тиоцетам, Гинкго-билоба, Прозерин, Тиоцетам, Милдронат, Кардонат, Магнерот, Никотиновая кислота, Цитрулина Малат).
- Глюкокортикоиды (Дефлазакорт, Преднизолон).
- Антихолинэстеразные препараты (Нивалин, Нейромидин, Прозерин, Оксазил, Галантамин).
- Ноотропные препараты (Луцетам, Церебролизин, Семакс, Когнитум).
Процедуры и операции
Физиотерапия/лечебная физкультура является важным компонентом лечения различного вида дистрофических процессов, например, при атаксии Фридрейха, что позволяет поддерживать тонус мышц и снижать болезненные проявления. Комплекс физиопроцедур и ЛФК подбирается конкретно при том или ином заболевании. При ряде заболеваний, сопровождающихся выраженными дистрофическими проявлениями, проводятся оперативные вмешательства, например, удаление хрусталика (при катаракте), ортопедические операции при исправлениях/деформациях костей стопы/пальцев верхней конечности.
У детей
Дистрофии у детей часто характеризуются не только не соответствующими возрасту изменениями физического развития, но и нарушением морфологического/функционально состояния внутренних органов, обменных процессов, иммунитета. Чаще они обусловлены различными хроническими расстройствами питания, крайним проявлением которых является квашиоркор. Нарушения питания у детей проявляется расстройствами метаболизма и отставанием ребенка в развитии в различных формах (гипотрофия, гипостатура, паратрофия). Дети дистрофики, в зависимости от формы и степени дистрофии имеют различные клинические проявления. Рассмотрим некоторые из них.
Гипотрофия
Встречается преимущественно у детей до 3-х лет, реже — в старшем возрасте. Основным появлением является недостаточность массы тела относительно роста ребенка. Выделяют несколько степеней тяжести:
- первая степень —дефицит массы тела варьирует в пределах 10 до 20%;
- вторая степень — недостаток веса составляет 20 — 30%;
- третья степень – недостаток веса превышает 30%.
Для гипотрофии первой степени характерно снижение тургора/истончение жирового слоя в области живота, бледность кожных покровов, сниженный аппетит. Гипотрофия второй степени проявляется шелушением кожных покровов, нарушениями активности, плохим аппетитом, отставанием в двигательном развитии, снижением тургора/эластичности тканей, практически полным исчезновением жирового слоя в зоне живота, туловища, конечностях при его сохранении на лице, одышкой, тахикардией, снижением АД. При этом у них резко повышается риск заболеть отитом, пневмонией, пиелонефритом.
Для третьей степени характерны атрофия жирового слоя на всей поверхности тела, атрофия мышц, низкий рост, отставание в психическом развитии. Из-за истощения западает родничок/глазные яблоки, образуются трещины в уголках рта, нарушается терморегуляция. Ребенок стремится к уединению, часто застывает подолгу в одной позе или вообще отказывается передвигаться. Лицо приобретает округлость, возникают отёки на голени, ягодицах, бёдрах, реже на лице, предплечье и кистях. Это крайняя степень, обычно белкового истощения, получила название квашиоркор. Как правило квашиоркор сопровождается жидким стулом, анемией, снижением рефлексов, иммунитета, что способствует присоединению инфекционных болезней. Иногда развиваются синдромы, которые могут угрожать жизни ребенка (острая сердечная недостаточность, дегидратация с токсикозом, гипотермия, гипогликемия, сопор, дистрофия печени и др.).
Гипостатура
Гипостатура характеризуется равномерным отставанием ребенка (массы и длины тела) от физиологически нормальных возрастных параметров. Гипостатура – расстройство питания в раннем детском возрасте, (обычно до года), проявляющееся неадекватными прибавками в весе и отставанием ребенка в росте. В среднем отставание ребенка в росте до года варьирует в пределах 5-10 см и 10-20 сантиметров у детей старшего возраста.
Соответственно и его масса тела соразмерна длине. Развивается при недостаточном поступлении белков, микроэлементов/витаминов в организм ребенка в период внутриутробного развития при несбалансированном питании матери, стрессах, токсикозах, фетоплацентарной недостаточности в период беременности или в первый год жизни при неправильном вскармливании (дефицит белков) или заболеваниях ребенка (энцефалопатии, рахит, врождённые пороки сердца, патологии развития головного мозга, наследственные/эндокринные заболевания).
Гипостатура у детей может определяться непосредственно после родов или через несколько месяцев. Дети, несмотря на миниатюрность имеют пропорциональное телосложение, но их параметры не соответствуют возрастным нормам, то есть биологический возраст отстает от календарного. Дети с гипостатура часто раздражительны, эмоционально лабильны, беспокойны, могут иметь извращенные пищевые привычки (употребление продуктов с определенным вкусом, только жидкой пищи и др.). Отмечается отставание в психомоторном развитии, реже — снижение интеллекта. Характерны нарушения сна, терморегуляции, задержка прорезывания зубов, созревания костной ткани. Кожа бледная, сухая, слабо развит подкожно-жировой слой, тургор снижен, стул неустойчивый, аппетит снижен. Рост медленный, прибавки массы тела незначительные.
Как поправиться? Лечение дистрофий заключается в устранение этиологических факторов, нормализации питания ребенка (диетотерапия) и ухода за ним. При необходимости проводится медикаментозное лечение. Диетотерапия предусматривает постепенное наращивание объема пищи до возрастных норм с соблюдение таких принципов как прием пищи небольшими порциями, увеличение частоты приема пищи, обязательный расчет количества БЖУ и каллоража в соответствии с возрастом, регулярный мониторинг состояния ребенка (табл. ниже).
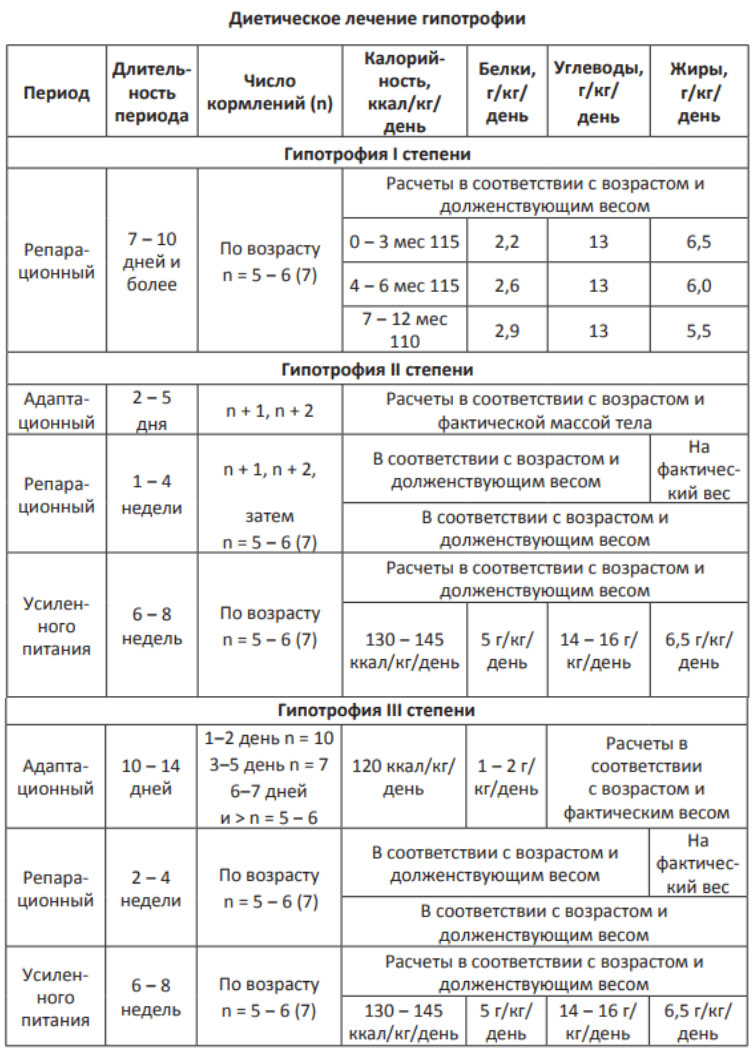
Могут использоваться специальные питательные смеси (Нутрилон пептиди СЦТ, Алфаре, Нутрилон пепти, Пентамен и другие). Медикаментозная терапия включает:
- Витаминотерапию (аскорбиновая кислота, B1-B6, курсы витаминов PP, A, B15, В5).
- Ферментотерапию (Панкреатин, Креон, Панцитрат и др.).
- Терапия, стимулирующая аппетит (Апилак).
- Препараты, улучшающие метаболизм (Глицин, Элькар, липоевая/янтарная кислота).
- Анаболики.
- Пробиотики (Лактобактерин, Бифидумбактерин, Аципол, Бифиформ и др.).
В случаях присоединения интеркуррентных заболеваний проводится соответствующая терапия. Основным показателем эффективности лечения является показатель прибавки массы тела. Оптимально, если этот показатель составляет/превышает 10 г/на кг/в сутки.
Диета
Как таковой единой диеты при дистрофии нет, однако диетическое питание при различного рода дистрофиях, сопровождающие множество болезней широко используется в их лечении. Диета подбирается в соответствии с конкретным заболеванием. Например, при жировой дистрофии печени — Диета при жировом гепатозе печени; при жировой дистрофии миокарда — Диета при ожирении; при дистрофии эпителия извитых канальцев почки — Диета при гломерулонефрите; при хроническом нарушении питания — Высокобелковая диета и так далее.
Профилактика
Какой-либо специфической профилактики дистрофий на сегодняшний день нет. Неспецифическая профилактика сводится к:
- Медико-генетической консультации в периоде планирования беременности для минимизации риска генетически обусловленных дистрофий.
- Обеспечению условий для нормального течения беременности.
- Полноценному грудному вскармливанию ребенка.
- Отказу от вредных привычек (злоупотребление алкогольсодержащими напитками, курение).
- Рациональному питанию в соответствии с физической активностью, возрастом и полом.
- Своевременной диагностике, адекватному лечению патологий/заболеваний, приводящих к дистрофии.
- Своевременному лечению любых инфекционных заболеваний.
- Активному образу жизни.
Последствия и осложнения
Последствия/осложнения дистрофий определяются ее видом и конкретной патологией/заболеванием, протекающих с явлениями дистрофии в том или ином органе, тканях.
Прогноз
Прогноз дистрофического процесса определяется множеством факторов — видом дистрофии, фактором воздействия и возможностью его устранения, конкретным заболеванием (формой и тяжестью его течения) и может варьировать в широких пределах от полного восстановления морфологической структуры ткани/органов и их функций (например, жировая дистрофия печени) до гибели органа с летальными исходами. При целом ряде дистрофий, особенно передаваемым по наследству, лечебные меры способствуют минимизации симптоматики заболевания, продлению жизни, но полного излечения на данном этапе развития медицины добиться невозможно.
Список источников
- Патологическая анатомия: Курс лекций. Учебное пособие. / Под ред. В. В. Серова, М. А. Пальцева. – М.: Медицина, 1998. – 640 с.
- Федотов В.П., Курбатов С.А., Иванова Е.А. и др. Клинико-электрокимографические критерии диагностики наследственных миотонических синдромов. Нервно-мышечные болезни 2012; (3): 55–66.
- Патологическая анатомия Акад. РАН М.А. Пальцев, проф. О.В. Зайратьянц – Москва, 2014 – с.19-42
- Наследственные атаксии и параплегии // С.Н. Иллариошкин // «Медицина». 2006.
- Шаймурзин М.Р., Евтушенко С.К. Новые современные технологии в терапии нервно-мышечных заболеваний, направленных на замедление их прогрессирования// Вестник физиотерапии и курортологии. - 2010.- №6. - С.40-41.






 Прозерин
Прозерин Пирацетам
Пирацетам Рибоксин
Рибоксин Нейромидин
Нейромидин Элькар
Элькар Глицин
Глицин Луцетам
Луцетам Метионин
Метионин Церебролизин
Церебролизин Преднизолон
Преднизолон Никотиновая кислота
Никотиновая кислота












Последние комментарии
Сергей: Здраствуйте! Подскажите где можно достать этот препарат Денебол гель?
Надежда: Наконец нашла эту статью, где рассказано как правильно питаться, после удаления желудка ...
Алла Анатольевна: Как только прочитаешь противопоказания, сразу сдохнуть хочется.
Елена: Мой опыт положительный. Я выпила эскапел, потом еще сделала тест, потом сделала узи и ...