Лимфолейкоз
Общие сведения
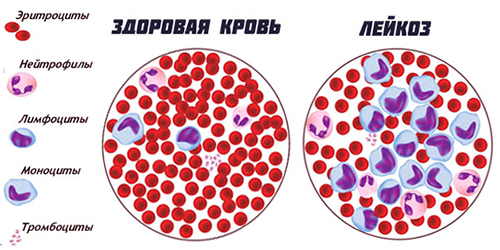
Лимфолейкоз, что это такое? Это злокачественное заболевание кроветворной системы, которое возникает вследствие мутации клеток иммунной системы лимфоцитов (в частности В-лимфоцитов).
Проявляется заболевание увеличением количества лимфоцитов (в костном мозге и крови), увеличением размеров печени, лимфоузлов и селезенки. Лимфоцитарный лейкоз является самой распространенной формой гемобластозов и относится к медленно текущим заболеванием, поэтому 40% не имеют показаний к началу лечения после установления диагноза.
В-клеточный лимфолейкоз может быть острым (называется лимфобластный лейкоз) и хроническим. Хронический лимфолейкоз считается болезнью пожилых (средний возраст 60-70 лет и старше), хотя последнее время эта форма лейкоза «помолодела» и встречается в возрасте 35-40 лет. У молодых лиц отмечается более короткий латентный период (от времени диагностики до начала лечения) — то есть имеет место более быстрое прогрессирование процесса. Чем старше по возрасту больные, тем чаще выявляется у них доброкачественная или «тлеющая» форма заболевания, отличающаяся спокойным течением. Но при этом у них появляются осложнения со стороны различных систем и заболевания воспалительного характера.
Между двумя формами — «тлеющей» и быстро прогрессирующей имеются варианты при которых успешно проводится цитостатическая терапия и прогрессирование сдерживается. Из всех форм чаще всего встречаются: прогрессирующая, доброкачественная, опухолевая, селезеночная. Рост распространенности данного гемобластоза вызывает необходимость активного поиска более эффективных методов лечения. Код хронического лимфолейкоза по мкб-10 C91.1.
Течению хронического лимфолейкоза сопутствует угнетение иммунной системы, а это приводит к риску появления инфекционных осложнений, особенно у пожилых. Нередко инфекционные осложнения являются первыми проявлениями этого заболевания. Сложность лечения состоит в том, проведение химиотерапии сопровождается снижением уровня нейтрофилов, что усугубляет иммунные нарушения. У пожилых по окончании полихимиотерапии наиболее часто присоединяются вирусные, бактериальные и грибковые инфекции, которые в 60% случаев являются причиной смертности.
Патогенез
Нормальные В-лимфоциты вырабатывают антитела, которые связывают антигены бактерий и вирусов. Чужеродные антигены микроорганизмов являются стимулами для развития лимфолейкоза. Субстратом опухоли являются клетки, которые контактировали с антигеном и превратились в клетки памяти. Постоянная антигенная стимуляция вызывает появление мутаций генов, в результате чего происходит неопластическая трансформация В-лимфоцитов и образование клона лейкемических клеток. Конечная стадия В-лимфоцита — плазматическая клетка, а при ХЛЛ вследствие мутаций лимфоциты не развиваются до плазматических клеток.
Клон измененных злокачественных клеток быстро пролиферирует. Пролиферация злокачественных клеток происходит в лимфатических узлах и в костном мозге в так называемых пролиферативных центрах. Образуется большое количество малых, зрелых лимфоцитов аккумулируется не только в костном мозге и крови, но и в лимфоузлах, селезенке, печени, вызывая лейкемическую инфильтрацию этих органов и нарушая их функции. При высокой скорости пролиферации болезнь будет иметь агрессивное течение. Однако установлено, что развитие ХЛЛ в большей части связано с накоплением малигнизированных лимфоцитов, которые долго живут, чем с их пролиферацией.
Классификация
В-клеточные опухоли:
- Острый лимфолейкоз (или острый лимфобластный лейкоз) относится к опухолям из предшественников В-лимфоцитов (незрелые лимфоидные клетки называются лимфобласты). При заболевании происходит их неконтролируемая пролиферация. Острый лимфолейкоз — самое распространённое злокачественное заболевание крови в детском возрасте.
- Хронический лимфолейкоз относится к опухолям с фенотипом зрелых лимфоцитов и характерен для лиц пожилого возраста.
Хронический лимфолейкоз
Различают следующие формы ХЛЛ:
- Доброкачественная.
- Прогрессирующая (или классическая).
- Опухолевая.
- Спленомегалическая.
- Костномозговая.
- Абдоминальная.
- Пролимфоцитарная.
Доброкачественная форма характеризуется очень медленным нарастанием лимфоцитоза, которое происходит на протяжении нескольких лет и даже десятилетий, параллельно с увеличением количества лейкоцитов. Уровень лейкоцитов обычно не превышает 30×109/л и очень редко достигает 50×109/л.
Лимфатические узлы при этой форме или не увеличены, или увеличены незначительно (только шейные и не больше 2 см). Такие больные не подлежат лечению, они находятся под наблюдением (каждые 3 месяца проводят исследования клинического анализа крови). Пациенты с этой формой трудоспособны, им только запрещаются работа во вредных условиях и повышенная инсоляция.
Прогрессирующая (или классическая) форма. В этой форме протекает в 45-50% случаев заболевания. Количество лейкоцитов и величина лимфоузлов нарастает с каждым месяцем. Увеличение количества лейкоцитов очень значительное — 500-1000×109/л. Одновременно увеличивается и количество лимфоцитов (в лейкоцитарной формуле они занимают 90%). Обнаруживаются зрелые формы лимфоцитов, но могут обнаруживаться 5-10% пролимфоцитов.
Уровень гемоглобина, эритроцитов и тромбоцитов в начальных стадиях нормальное. Одновременно увеличиваются лимфоузлы. Потом присоединяется увеличение селезенки, которая редко достигает очень больших размеров. Несколько позже увеличивается и печень. В некоторых случаях проявления заболевания в виде увеличения перечисленных органов отсутствуют даже при очень высоком лейкоцитозе и лимфоцитозе.
Опухолевая форма проявляется значительным увеличением лимфоузлов, которые имеют плотную консистенцию, при относительно невысоком лейкоцитозе (20-50×109/л). Увеличение селезенки чаще умеренное. Миндалины увеличены и практически смыкаются. При такой значительной гиперплазии лимфатической ткани интоксикация длительное время мало выражена. В костном мозге не более 20-40% лимфоцитов. Для опухолевой формы характерно:
- Увеличенные лимфоузлы, которые сливаются, образуя конгломераты. Сначала увеличиваются шейные, подмышечные и паховые, потом паратрахеальные со сдавлением трахеи и бронхов. У некоторых пациентов определяются увеличенные внутрибрюшные ЛУ.
- Лимфоцитарная инфильтрация костного мозга.
- Быстро прогрессирующее течение, выживаемость не более 3 лет. Опухолевая форма является основанием для цитостатической терапии.
Селезеночная форма протекает с преимущественным увеличением селезенки. При этом лимфатические узлы увеличены умеренно, а уровень лейкоцитов может быть различным, нарастающим на протяжении месяцев. Селезенка у больных занимает почти всю брюшную полость и вызывает сдавливание других органов и болевой синдром. Нередко не значительно увеличивается печень. Часто встречается гемолитическая анемия. Выживаемости составляет 5 лет. Абдоминальная форма характеризуется увеличением только лимфоузлов брюшной полости на протяжении месяцев и лет. Для выявления этой формы заболевания применяется УЗИ и КТ.
Пролимфоцитарная форма отличается, строением лимфоцитов, которые имеют крупную нуклеолу. Очень часто выявляются хромосомные аномалии, эта форма быстро прогрессирует и плохо поддается лечению. Продолжительность жизни — 3 года. Основные особенности пролимфоцитарной формы:
- склонность к геморррагиям;
- возраст старше 70 лет;
- значительное увеличение селезенки;
- увеличение лимфоузлов незначительное;
- инфильтрация кожи лейкемическими клетками, которая проявляется папулезной сыпью в области лица, рук, туловища;
- анализ крови: лимфоциты 100×109 /л и половина из них — пролимфоциты.
Костномозговая форма характеризуется прогрессирующей панцитопенией и практически полным замещение костного мозга зрелыми лимфоцитами. При этом лимфоузлы, селезенка и печень не увеличены. Прогноз очень неблагоприятный.
В-клеточный лимфолейкоз различается по степеням, которые отражают естественное течение заболевания и постепенное увеличение опухолевой массы в различных органах. Классификация по K. Rai отражает это и позволяет прогнозировать течение заболевания и выживаемость пациентов.
Хронический лимфолейкоз 1 степени характеризуется лимфоцитозом, также при 1 стадии отмечается увеличение лимфатических узлов. Выживаемость 9 лет.
Хронический лимфолейкоз 2 степени протекает лимфоцитозом, увеличением лимфатических узлов и дополнительно при 2 стадии отмечается увеличение селезенки и/или увеличение печени. Средняя выживаемость 6 лет.
Хронический лимфолейкоз 3 степени характеризуется лимфоцитозом и снижением гемоглобина меньше 100 г/л. Снижение гемоглобина при 3 стадии свидетельствует о вовлечении в процесс костного мозга и является основным критерием независимо от увеличения органов и лимфоузлов. Выживаемость в этой стадии составляет 1,5 года.
Хронический лимфолейкоз 4 степени является самым неблагоприятным: помимо лимфоцитоза 4 стадия характеризуется снижением уровня тромбоцитов менее 100×109/л, что грозит развитием кровотечений, в том числе и смертельных для больного. Тромбоцитопения является определяющей для этой стадии независимо от увеличения органов и лимфоузлов. Выживаемость составляет не более 1,5 лет.
Причины
Как известно, канцерогены играют значение в развитии многих онкологических заболеваний, однако не установлено связи между их действием и развитием хронического лимфолейкоза. Связь этого заболеваниями с излучением, вирусами, питанием также не доказана. Тем не менее, доказано, что постоянный контакт с пестицидами и инсектицидами повышает риск развития заболевания.
Предрасположенность к ХЛЛ передаётся по наследству и доказано, что риск развития данного заболевания у непосредственных родственников выше в 8,5 раз, чем в общей популяции людей. Причем во втором поколении отмечается более ранее развитие болезни и более быстрое прогрессирование. При изучении хромосомных нарушений выявили, что они проявляются в виде дополнительной хромосомы 12 и делеции хромосом 6 и 13, 11.
Симптомы лимфолейкоза
Симптомы хронического лимфолейкоза отличаются большим разнообразием и во многом зависят от возраста больных. У одних заболевание протекает спокойно, и больные длительное время не нуждаются в лечении. У других — процесс протекает бурно и тяжело, поэтому требуется немедленное начало лечения.
Одной из причин такого разнообразия течения являются возрастные особенности больных. У лиц пожилого возраста чаще отмечается «застывшая», не прогрессирующая, вялотекущая форма, при которой симптомы не меняются на протяжении многих лет — это может быть 20-30 лет. В молодом возрасте наблюдается прогрессирующее течение и высокая встречаемость опухолевых форм.
Вначале жалобы неспецифичны: слабость, повышенная потливость, снижение веса, частые простудные заболевания. На этой стадии гемобластоз выявляется случайно при обращении к врачу по различным поводам. В дальнейшем основные симптомы хронического лимфолейкоза у всех пациентов включают увеличение лимфоузлов селезенки и печени. Сначала происходит незначительное увеличение узлов в определенной последовательности: шейные, затем подмышечные, паховые и другие группы.
Первое увеличение узлов может быть связано с респираторными заболеваниями, когда обнаруживаются увеличенные узлы на шее. В это же время может появиться «заложенность» в ушах и ухудшиться слух, что связано с разрастанием лимфатической ткани в евстахиевых трубах, которая отекает при инфекции. Наибольшие размеры узлов отмечаются у лиц молодого возраста — размеры шейных, подмышечных, могут достигать 4-5 см и превращаться в конгломераты.
Лимфоузлы, независимо от возраста, эластичны, подвижны (за исключением «пакетов» узлов) и безболезненны. Увеличение абдоминальных и забрюшинных чаще отмечается у лиц молодого возраста. Умеренное увеличение селезенки наблюдается у молодых пациентов, а значительная спленомегалия — у пожилых. Селезенка у них достигает громадных размеров, опускаясь в малый таз. Объясняется это тем, что у молодых лиц преобладает инфильтрация опухолевыми клетками узлов, у пожилых — селезенки, увеличение которой проявляется тяжестью или дискомфортом, а также ранним насыщением. Увеличение печени проявляется тяжестью, возможны тошнота, снижение аппетита и отрыжка.
За счёт скопления опухолевых клеток в костном мозге и угнетения нормального кроветворения на поздних стадиях развивается анемия, проявляющаяся головокружением, кровоизлияниями и кровотечениями из-за снижения уровня тромбоцитов. Характерно выраженное угнетение иммунитета, поэтому появляется предрасположенность к инфекциям (простудные заболевания, пиодермии, пневмонии).
Терминальная стадия характеризуется прогрессирующим ухудшением состояния, истощением, интоксикацией, отсутствием аппетита, повышением температуры. Повышение температуры может быть связано и с самим заболеванием, а также с тяжелой пневмонией или туберкулезом легких. Тяжелая генерализованная инфекция очень характерна для терминальной стадии и является причиной их смерти. Возможна инфекция кожи и мочевыводящих путей. Герпетическая инфекция также может присоединиться на любой стадии, но чаще в терминальной.
Один из грозных признаков терминальной стадии — почечная недостаточность, которая связана с инфильтрацией ткани почек лейкозными клетками. Проявляется уменьшением выделения мочи, а в крови значительно повышается содержание мочевины и остаточного азота. В терминальной фазе также возможно появление нейролейкемии, которая проявляется головными болями, рвотой, периферическими параличами. При лимфоидной инфильтрации легких развивается выраженная одышка и дыхательная недостаточность.
Характерным признаком конечной стадии является анемия, которая связана лимфоидной инфильтрацией костного мозга и вытеснением красного кроветворного ростка. Анемия проявляется выраженной слабостью, одышкой, головокружением. У некоторых больных развивается бластный криз и происходит трансформация ХЛЛ в другие лимфопролиферативные заболевания (синдром Рихтера, плазмаклеточный лейкоз, пролимфоцитарный лейкоз, миеломная болезнь).
Анализы и диагностика
- Клинический анализ крови. Анализ крови при лимфолейкозе выявляет характерное для данного заболевания повышение уровня лейкоцитов за счет лимфоцитов (лимфоцитоз). Среди лимфоцитов преобладают зрелые, малые. Лейкоцитоз колеблется от 5×109/л до 10×109/л, что является достоверным признаком заболевания, но в большинстве случаев лейкоцитоз достигает 20-50х109/л. Если есть высокий лейкоцитоз 100-500х109/л при первом обращении больного к врачу, то это свидетельствует о длительном не диагностированном периоде. В анализе крови выявляют небольшое количество пролимфоцитов (2–3%), а у некоторых больных единичные лимфобласты (1–2%). Характерным признаком является обнаружение клеток Боткина-Гумпрехта (разрушенные ядра лимфоцитов) в разном количестве. Показатели анализа крови при лимфолейкозе, в частности значительное увеличение количества лейкоцитов и лимфоцитов, указывают на высокую активность опухолевого процесса и объясняют быстрое прогрессирование заболевания. Картина крови меняется: лимфоцитоз постепенно нарастает, если в начальных стадиях лимфоциты составляют 60-70%, то в конечной стадии заболевания 90% и более, что бывает при тотальном замещении лимфоцитами костного мозга. У многих пациентов длительное время может быть только лимфоцитоз (40-50%) при значении лейкоцитов на верхнем пределе нормы. Уровень гемоглобина и тромбоцитов чаще всего нормальный, но при высоком лейкоцитозе отмечается снижение этих показателей.
- Исследование пунктата костного мозга. На ранних этапах обнаруживают небольшое увеличение процента лимфоцитов в миелограмме (30-50%), а в поздних стадиях лимфоциты составляют 95% костномозговых элементов. Для лиц молодого возраста, по сравнению с пожилыми, характерно сохранение эритро и гранулоцитопоэза.
- Иммунологическое исследование. Лимфоциты при ХЛЛ имеют характерный иммунофенотип — на поверхности опухолевых клеток обнаруживают антигены CD19, CD5, CD23 и в небольшом количестве антигены CD20 и CD22.
- Для выявления мутаций хромосом проводят цитогенетическое исследование, которое выявляет дополнительную хромосому 12 и делеции хромосом 6 и 13, 11.
Лечение лимфолейкоза
В отличие от других лейкозов, лечение ХЛЛ не всегда требует немедленного начала. Особенно это касается начальных стадий заболевания и доброкачественном течении. В этот период придерживаются тактики «наблюдай и жди». Необходимость лечения возникает только при активных проявлениях: слабость, гиперлейкоцитоз (удвоение количества лейкоцитов менее, чем за 5-6 месяцев, быстрое увеличение селезенки и лимфоузлов, снижение уровня эритроцитов и тромбоцитов). Стандарт лечения — различные химиотерапевтические режимы. Поскольку ХЛЛ — неизлечимое заболевание, целью лечения является достижение длительных ремиссий и повышение качества жизни пациента. С учетом системности заболевания лучевая терапия не применяется.
Выбор режимов зависит от распространенности процесса, возраста, степени активности, тяжести сопутствующих заболеваний. С учетом этих факторов все пациенты делятся на на несколько категорий:
- пациенты, находящиеся на ранних стадиях и не имеющие признаков прогрессирования;
- больные молодого возраста, имеющие распространенные стадии заболевания без тяжелой сопутствующей патологии;
- пациенты пожилого возраста и молодого возраста, имеющие распространенные стадии и тяжелую сопутствующую патологию;
- больные очень высокого риска.
Первыми химопрепаратами, которые использовали при лечении этого заболевания, были алкилирующие препараты — хлорамбуцил (Лейкеран), потом стали использоваться пуриновые аналоги (Флударабин-Тева, Флудара, Веро-Кладрибин), которые давали ремиссию на 1-1,5 года.
 Более новые препараты с действующим веществом бендамустин (Рибомустин, Ковада, Розустин) являются также химиопрепаратами, но сочетают в себе свойства алкилирующих препаратов и аналогов пурина. В механизме его действия важно то, что он прочно связывается с ДНК опухолевой клетки и продолжает оказывать действие после выведения из крови. Другое преимущество — он в малом количестве выводится почками, поэтому назначается при нарушении их функции. Лучшие результаты стали получать при сочетании Флударабина и Циклофосфана, что позволило достигать 33% больных пятилетних ремиссий.
Более новые препараты с действующим веществом бендамустин (Рибомустин, Ковада, Розустин) являются также химиопрепаратами, но сочетают в себе свойства алкилирующих препаратов и аналогов пурина. В механизме его действия важно то, что он прочно связывается с ДНК опухолевой клетки и продолжает оказывать действие после выведения из крови. Другое преимущество — он в малом количестве выводится почками, поэтому назначается при нарушении их функции. Лучшие результаты стали получать при сочетании Флударабина и Циклофосфана, что позволило достигать 33% больных пятилетних ремиссий.
Следующий этап в лечении данного заболевания связан с применением препаратов моноклональных антител, которые относятся к таргетным (таргет в переводе — мишень или цель) препаратам. Это молекулярно-нацеленные препараты, которые действуют на определенные мишени — белковые молекулы, участвующие в канцерогененезе. Лечение моноклональными антителами называют иммунотерапией.
Эти препараты делают противоопухолевую терапию наиболее эффективной. Действие иммунотерапии высокоизбирательно и практически отсутствует токсичность. В настоящий момент для лечения данного заболевания применяются ритуксимаб (Мабтера) и алемтузумаб (Кэмпас). Препарат КЭМПАС – это новый этап развития моноклональных антител. При его применении стало возможным говорить об излечении хронического лимфолейкоза — он уничтожает опухолевые клетки в крови и в костном мозге.
Препараты моноклональных антител стали вводиться в режимы терапии. Лучшие результаты получают при сочетании Флударабина и Мабтеры, но наиболее эффективной оказалось сочетание: ритуксимаб (Мабтера), флударабин и циклофосфан (схема РФЦ), которая применяется у ранее не леченных больных и для повторного лечения при рецидиве. Более перспективно применение второго вида моноклональных антител — препарат Кэмпас, который вызывает значительное уменьшение лимфоцитов в крови, селезенке и костном мозге. При этом нужно помнить, что нее всегда имеются показания и необходимость назначения таргентных препаратов — в одних случаях они просто улучшают общую картину лечения, а в других — являются действительно необходимыми, имеют решающее значение и без них невозможно лечение.
Лечение больных молодого возраста, имеющих распространенные стадии и при отсутствии тяжелых сопутствующих заболеваний.
Эффективность алкилирующих препаратов (Лейкеран), который применяется в монорежиме, остается невысокой: частичная ремиссия достигается у 50-60%. Эффективность Флударабина в монорежиме значительно превышает эффективность предыдущего препарата и возможно достижение полного ответа на лечение у трети больных. Наиболее эффективен режим FC (сочетание Флударабин и Циклофосфамид).
Также применяются режимы полихимиотерапии — СОР (циклофосфан, винкристин, преднизолон) и СНОР (доксорубицин + циклофосфамид + винкристин + преднизолон). Более новым методом лечения стало добавление к флударабин-содержащиму режиму моноклонального антитела ритуксимаба — режим FR. Также возможен режим BR (бендамустин + ритуксимаб).
В настоящее время стандартом первой линии является терапия: флударабин, циклофосфамид и ритуксимаб (режим FCR), который эффективен в 95% случаев, но он обладает токсичностью, поэтому можно применять только у больных без сопутствующих заболеваний. Таким образом, больным молодого возраста, не имеющих сопутствующих заболеваний, могут применяться режимы: FCR, FR, BR.
Лечение больных молодого возраста, имеющих распространенные стадии, при наличии тяжелых сопутствующих заболеваний.
При наличии выраженной сопутствующей патологии при лечении используется ритуксимаб (Мабтера) в сочетании с хлорамбуцилом (Лейкеран), бендамустином (Рибомустин), кортикостероидами (Преднизолон).
Больным с сопутствующей патологией, но при отсутствии делеции 11q (или 17p) применяют: ритуксимаб в сочетании с хлорамбуцилом (Лейкеран), бендамустином (Рибомустин), флударабином (Флудара, Веро-Флударабин), кортикостероидами (Преднизолон) и монотерапия алемтузумабом (Кэмпас). У пациентов с наличием делеции 11q и сопутствующей патологии из схемы убирают флударабин, а также назначают режим FCR-light и алемтузумаб (Кэмпас).
Лечение больных пожилого возраста с наличием сопутствующих заболеваний
У данной группы больных первой линией лечения считается хлорамбуцил (Лейкеран) в монотерапии, дающая выживаемость без прогрессирования 18 мес. Сочетание хлорамбуцила и флударабина, что показывает более высокий общий ответ на лечение, но не улучшает выживаемость. Флударабин не назначается в возрасте больше 70 лет. Поэтому препаратом выбора у лиц, которым не показаны схемы с флударабином, является хлорамбуцил, поскольку он обладает меньшей гематологической токсичностью.
Эффективной является комбинированная терапия: хлорамбуцил + ритуксимаба, которая эффективнее монотерапии хлорамбуцилом (выживаемость без прогрессирования 23,9 мес). Данная комбинация назначается больным, которым более интенсивные режимы (например, FCR с флударабином) нельзя назначать.
Бендамустин в виде монотерапии также рекомендован для лечения пациентов, которым не показаны флударабин-содержащие режимы. Длительность стойкой полной ремиссии после его применения в 3 раза больше по сравнению с приемом хлорамбуцила. В связи с этим, бендамустин более предпочтительный препарат чем хлорамбуцил, если нельзя использовать полную схему FCR (флударабин, циклофосфамид и ритуксимаб).
Лечение больных группы высокого риска
К группе высокого риска относятся больные, которые:
- не ответили на лечение флударабином;
- дали рецидив в течение года по окончании курса флударабином;
- дали рецидив в течение 2 лет после использования флударабина.
Больным этой группы должна проводиться аллогенная трансплантация.
Группа очень высокого риска включает:
- пациентов рефрактерных к флударабину;
- пациентов с рецидивами через 2 года после схемы FCR;
- наличие делеции р53 и делеции 17p13.
Последняя группа больных относятся к очень неблагоприятной категории — возможности лечения в этой группе очень ограничены. Наиболее эффективным является применение алемтузумаба (Кэмпас), кортикостероидов (пульс терапия метилпреднизолоном), или комбинации этих двух групп, а также брентуксимаб-содержащих схем и трансплантации стволовых клеток для закрепления лечения первой линии.
В лечении данного заболевания с каждым годом происходит прогресс и появляются новые не химиотерапевтические препараты, применением которых можно добиться если не полного излечения, то длительной выживаемости. К таким препаратам относится ингибитор тиразинкиназы Брутона ибрутиниб (препарат Имбрувика — первое поколение ингибиторов). Посещая форум, все чаще встречаются отзывы об эффективности этого препарата, который не входит в федеральные программы лечения и больные приобретают его самостоятельно.
Акалабрутиниб (препарат Калквенс) — также ингибитор тиразинкиназы, но нового поколения. В январе 2019 года получено разрешение FDA (Управление по контролю за пищевыми продуктами и лекарственными средствами США) на комбинированное использование Калквенса и Газивы, а также применение Венклекста (ингибитор антиапоптозного белка) с Газивой. Минздрав РФ одобрил лечение препаратом Венклекста в комбинации с Мабтерой для пациентов с рецидивирующим или рефрактерным лимфолейкозом и наличием делеции 17p. Это не химиотерапевтические препараты и являются первой комбинацией для перорального приема. Для больных с делецией 17р препаратом выбора является Кэмпас, который применяется в монорежиме и вместе с флударабином.
Доктора
Лекарства
- Противоопухолевые препараты: Лейкеран, Рибомустин, Ковада, Флударабин-Тева, Флудара, Веро-Кладрибин.
- Моноклональные антитела: Мабтера, Кэмпас, Газива, Ритуксан, Мабкампат, Герцептин, Авастин, Эрбитукс.
- Ингибиторы тиразинкиназы: Брутона, Имбрувика, Калквенс.
Процедуры и операции
Трансплантация стволовых клеток имеет важное значение в лечении больных. Может применяться аллогенная и аутологичной трансплантации. При аутологичной источником гемопоэтических стволовых клеток является сам пациент. Заготовка клеток проводится во время лечения, и они подвергаются криоконсервации. При аллогенной трансплантации клетки получают от родных братьев, сестер или от совместимого неродственного донора. Аллогенная трансплантация может привести к полному излечению, но недостатком ее являются осложнения вследствие отторжения трансплантата (реакция «трансплантат против хозяина»). Высокая токсичность аллогенной трансплантации ограничивает возможности его применения.
АллоТКМ имеет высокий излечивающий потенциал и позволяет длительно контролировать заболевание. Важным фактором, который влияет на решение о проведении аллоТГСК, является отсутствие ответа на терапию. У пациентов с хромосомными аберрациями (делеции р53 и делеции 17p13) аллогенная трансплантация проводится в первой линии лечения. После аллогенной трансплантации снижается частота рецидивов, в отличие от аутоТГСК.
АутоТГСК проводится для закрепления первой или второй ремиссии. Она не имеет существенного преимущества перед стандартной химиоиммунотерапией, поэтому не является стандартом оказания помощи. АутоТГСК может применяться отдельных случаях, например при синдроме Рихтера.
Диета
Правильное питание при лимфолейкозе хроническом позволяет поддерживать здоровье больного. Питание должно быть сбалансированным по основным веществам. Больные нуждаются в полноценной белковой пище, особенно после химиотерапии. Можно употреблять нежирное мясо, птицу, рыбу, молочные продукты. Источниками растительного белка являются орехи, соевые продукты и другие бобовые, которые можно умеренно употреблять при хорошей переносимости (при отсутствии вздутия кишечника).
Углеводы являются источником энергии, поэтому для восполнения энергетических затрат больные должны употреблять преимущественно сложные углеводы: фрукты, хлеб, овощи, злаки. Жиры в рационе должны быть представлены растительным маслом (полезны масла холодного отжима с высоким содержанием омега-3 жирных кислот — льняное), орехами, рыбьим жиром. В рационе должны преобладать овощи, фрукты и продукты из цельного зерна. В каждый прием пищи нужно включать 150 г овощей или фруктов (общее количество за день 500-600 гр). По рекомендации врача в рацион пациента может быть дополнительно введен комплекс витаминов и микроэлементов.
Общие принципы питания выглядят так:
- Увеличить потребление злаков, фруктов, овощей, орехов.
- Преимущественное употребление рыбы и полезных масел.
- Дробное питание.
- Следить за питьевым режимом. При отсутствии противопоказаний употреблять очищенную воду до 2 л в день.
- Отказаться от тугоплавких жиров.
- Ограничить употребление простых углеводов (сахар, конфеты, варенье, джемы, сладкая выпечка).
- Исключить жареную и копченую продукцию.
- Недопустимо употребление продуктов с пищевыми добавками.
Профилактика
Специфической профилактики данного заболевания не существует. Важно вести здоровый образ жизни, который включает физическую активность, пребывание на природе, правильное питание, исключение, по возможности, вредных факторов на производстве и в быту. Необходимо проходить профилактические осмотры с обязательной сдачей анализа крови и флюорографическим обследованием.
Больные с I-II стадией ХЛЛ являются трудоспособными, но для профилактики прогрессирования заболевания им противопоказаны:
- физический труд средней тяжести и тяжелый;
- нервно-психическое напряжение;
- работа, связанная с вибрацией, вынужденным положением тела, контактом с ионизирующей радиацией, токсическими факторами, гематоксичными ядами, неблагоприятными микроклиматическими производственными условиями.
Последствия и осложнения
Осложнения делятся на аутоиммунные и инфекционные. Как первые, так и вторые могут развиваться в любом периоде заболевания. Среди аутоиммунных выделяют:
- Аутоиммунная гемолитическая анемия. Иногда бывает самым ранним симптомом и появляется задолго до других признаков. Но все-же чаще развивается уже при выраженной клинико-гематологической картине заболевания.
- Аутоиммунная тромбоцитопения (синоним идиопатическая тромбоцитопеническая пурпура). Встречается у 3% больных. Характеризуется быстрым снижением тромбоцитов (30×109/л). Если количество тромбоцитов быстро снижается вместе с развитием анемии, то вероятнее всего тромбоцитопения имеет аутоиммунный характер. Появляются признаки геморрагического диатеза: кожные кровоподтеки, носовые кровотечения и кровотечения из десен. Большую опасность представляют кровоизлияния в головной мозг, которые становятся причиной смерти.
- Парциальная красно-клеточная аплазия. Характеризуется тяжелой анемией.
Проблема инфекционных осложнений имеет решающее значение для течения и исхода хронического лимфолейкоза. Инфекционные осложнения возникают на любом этапе болезни и встречаются у 75-80% больных. У большей части больных они становятся причиной смерти. Чаще с инфекционными осложнениями врачи сталкиваются у больных с выраженными проявлениями основного заболевания. Нередко встречается наличие 2-3 инфекционных очагов. Лечение инфекционных осложнений у этих больных представляет большие трудности.
Среди инфекционных осложнений наиболее часто встречаются:
- Заболевания дыхательных путей: пневмонии, трахеиты, бронхиты, плевриты. У некоторых больных воспаление легких бывает два раза в год и протекают тяжело.
- Нагноительные поражения кожи — рожа, фурункулез, пиодермия. Если инфекционные очаги быстро не ликвидируются, часто процесс распространяется. На месте инъекции возникает абсцесс, потом нагнаиваются лимфатический узел, затем появляется абсцесс подкожной клетчатки, септикопиемия и тяжелая пневмония.
- Herpes zoster. Течение этого вирусного заболевания очень тяжелое. Начинается с повышения температуры и появления сильных болей в области грудной клетки или конечностей. Затем появляются кожные элементы (пузырьки) в этих местах, а у некоторых больных и на лице. Множественные пузырьки могут полностью покрывать кожу туловища, лица и конечностей. У некоторых больных бывает буллезная форма, когда размеры пузырей достигают 15-20 см.
- Инфекция мочевыводящих путей (цистит, пиелонефрит).
Прогноз при лимфолейкозе
Как и при любом онкологическом заболевании прогнозы на выздоровление при лимфолейкозе не делаются. Речь идет о длительном безрецидивном периоде и возможности вернуться к обычной трудовой деятельности. Создание новых препаратов и дальнейшие разработки дают уверенность в том, что возможно будет полное выздоровление больных, но на сегодняшний день оно не достигается даже пересадкой костного мозга.
Прогноз при хроническом лимфолейкозе зависит от стадии на момент выявления заболевания. Пациенты с 0-II стадией имеют большую продолжительность жизни, чем больные в III- IV стадиях. Выживаемость без лечения при 0–II стадиях составляет 5–20 лет, а больные III–IV стадий умирают в течение 3-4 лет. Выживаемость больных, проходивших лечение, предопределяет лечение первой линии — чем эффективнее были режимы, тем благоприятнее исход.
Также прогноз зависит от наличия хромосомных изменений и маркера CD 38, что является неблагоприятным признаком. Продолжительность жизни при хроническом лимфолейкозе с наличием делеции 13q составляет 10 лет. Продолжительность жизни при трисомии 12-9 лет, еще короче она при делеции 11q — 6 лет, а самая короткая при делеции 17р — всего 2,5 года. В клинике делеция 13q соответствует непрогрессирующей форме, и такие больные не нуждаются влечении, а больные с делецией 17р рано получают лечение, но оно оказывается либо неэффективным, либо дает кратковременный эффект.
Если до начала 90-х годов ХХ в. выживаемость при активной форме болезни была не более 3-4 лет, то сейчас применяются средства, которые позволяют получать ремиссии, по длительности больше (7 и более лет), чем показатели выживаемости в 90-х годах. Об этом свидетельствуют отзывы больных. Эффективным подходом является применение моноклональных антител (алемтузумаб), кортикостероидов и брентуксимаб-содержащих режимов.
Список источников
- Крячок И.А. Хронический лимфолейкоз: новое в лечении. Подходы к терапии первой линии и их эволюция/Клиническая онкология. Онкогематология №3(11) 2013.
- Бессмельцев С.С., Волкова М.А., Абдулкадыров К.М./Флударабин в лечении хронического лимфолейкоза/ Гематология и трансфузиология.— 2004.-N 3.-С.6-11
- Волкова МА. Хронический лимфолейкоз. В: Клиническая онкогематология (руководство для врачей). М: Медицина, 2001: 376–92.
- Волкова М.А. Полвека в терапии хронического лимфолейкоза. Гематология и трансфузиология 1998; 5: 6–12.
- Яхнина Е.И., Никитин Е.А., Асцатуров И.В. и др. Доброкачественная форма хронического лимфолейкоза. Терапевтический архив 1997; 7: 11–7.





 Лейкеран
Лейкеран Мабтера
Мабтера















Поставлен диагноз ХЛЛ с 2009 года. Пройдено 12 курсов химии "мабтера,ритуксинаб".После первых 6 курсов химии ремиссия составила 4 года. в последствии после очередных 6 курсов ремиссия 2 года. Сейчас назначен препарат "Калквенс" -акалобрутиниб.Принимаю в течении 4-х месяцев 2 раза в сутки. Лейкоциты "прыгают" то 116,то 70ед и обратно. Появлялись сильные кровоподтёки под кожей,в глазах 3 раза лопаются капиляры . Состояние в целом не улучшается. Интересует вопрос , будет улучшение или просто на нас проводят опыты ?