Фенилкетонурия
Общие сведения
Фенилкетонурия относится к наследственным заболеваниям из группы ферментопатий. Она связана с нарушением обмена ароматических аминокислот, а конкретно — фенилаланина. Если человек с этим заболеванием не соблюдает низкобелковую диету, то в его организме происходит накопление фенилаланина и продуктов метаболизма, обладающих токсическим действием на ЦНС, которое в свою очередь вызывает поражения нервных структур и приводит к нарушениям умственного развития. Возникает фенилпировиноградная олигофрения по аутосомно-рецессивному типу наследования, однако на сегодняшний день это одно из немногих наследственных заболеваний, которое поддается успешному лечению.
Распространённость не зависит от гендерного различия, но отличается у разных групп населения. Однако, риску летального исхода более подвержены мальчики возрастом до 1 года.
В европеоидной расе и среди жителей Америки фенилкетонурия встречается у 1 человека на 10-15 тыс. Наиболее высокая частота случаев зарегистрирована у граждан Турции: 1 из 2,60 тыс. Финляндия и Япония отличается наиболее низкой частотой встречаемости данного недуга не более 1 человека на 120 тыс. рождений. Сенсацией были данные исследований 1987 г, когда среди представителей цыганских популяций в Словакии был обнаружен сверхвысокий уровень фенилкетонурии, вызванный предположительно инбридингом: болезнь выявляли у каждого 4-ого ребенка.
Историческая справка
В 1934 г норвежским врачом Иваром Асбьёрном Феллингом была выявлена гиперфенилаланинемия. Она оказалась ассоциирована с задержкой умственного развития. У жителей Норвегии заболевание называлось в честь его открывателя — болезнь Фёллинга.
Методика успешного лечения фенилкетонурии впервые была разработана в стенах Бирмингемского детского госпиталя (Англия). Ее разработал Хорст Биккель со своей командой медиков в начале пятидесятых годов двадцатого века. Однако, больший успех терапия имела, когда удалось широко применять раннюю диагностику недуга, вызванного повышенным содержанием фенилаланина в кровяном русле новорождённых по методу Гатри, разработанному и внедренному в 1958-1961 годах.
Фенилкетонурия, что это за заболевание?
Название происходит от двух названий химических соединений – фенилаланина и кетонов, а также греческого слова uron означающего – моча. Это заболевание вызывает расстройства движений и тонуса мышц, а также отставание физического развития и прогрессирующее слабоумие, поэтому еще называется фенилпировиноградной олигофренией.
На начальных этапах фенилкетонурия никак себя не проявляет и протекает бессимптомно. Тревожными знаками становится манифестация симптомов в виде сонливости и плохо аппетита у детей 6-12 месяцев. Такие дети отличаются от родственников и ровесников слишком светлой кожей, блондинистыми волосами и голубым цветом глаз. Также характерным симптомом становится развитие сыпи, напоминающей дерматит или экзему. Отсутствие лечения приводит к заметной, значительно выраженной задержке умственного развития, поэтому очень важно выявить болезнь на первых годах жизни, пока не успели произойти необратимые патологические изменения.
Патогенез
Как незаменимая аминокислота – фенилаланин является протеиногенной и играет важную роль в построении белковых молекул всех живых организмов, обеспечивая стабилизацию белковых структур и фолдинг (нативную укладку), являясь составным звеном функциональных центров. Необходим для синтеза гормонов щитовидной железы (в большей мере — тироксина), а также адреналина и меланина.
Метаболический блок превращения фенилаланина в тирозин приводит к его накоплению и активации побочных путей его обмена (например, печенью), в результате чего в тканях организма аккумулируются его токсичные производные — фенилпировиноградная, фениломолочная и другие кетоновые кислоты, в норме которых практически не должно образовываться. Помимо этого, происходит синтез ортофенилацетата и фенилэтиламина – соединений также почти полностью отсутствующих при нормальном метаболизме, причем производные последнего являются психоделиками и психостимуляторами. Наличие их в избытке инициирует нарушение обмена жиров в структурах головного мозга. Считается, что именно этот фактор вызывает прогрессирующее снижение интеллекта и может привести в самой глубокой степени умственной отсталости — идиотии. На сегодняшний день остаются до конца невыясненными механизмы развития нарушений работы мозга, вызванные фенилкетонурией. Предположительно, этому способствует дефицит нейромедиаторов (серотонина, дофамина) в синапсах мозга на фоне прямого токсического действия фенилаланина и относительного снижения количества тирозина и прочих «крупных» аминокислот, способных конкурировать с фенилаланином в процессах переноса через гематоэнцефалический барьер.
Гиперфенилаланинемия приводит к нарушениям обмена липо- и гликопротеидов, аминокислотного равновесия как жидкостных сред, так и клеточных структур. В основе клинических проявлений также лежат нарушения метаболизма гормонов, обмена моноаминовых нейромедиаторов таких как катехоламины и серотонин.
Разлад функции печени выражен в виде диспротеинемии, генерализованной гипераминоацидемии, метаболического ацидоза, нарушения белковосинтезирующей и окислительной деятельности клеточных органелл.
Классификация
Различают типичную (классическую) и атипичные формы (варинатные, коферментзависимые, злокачественные — на них приходится примерно 10% случаев) фенилкетонурии в связи с генетической и клинической неоднородностью аномалий обмена фенилаланина, а также кофактора — биоптерина.
Причиной второй диеторезистентной атипичной формы фенилкетонурии является дефицит дигидроптеридинредуктазы в результате генного дефекта локализующегося на участке 4р 15.3 хромосомы. Открыл ее Смит в 1974 году. Энзимный дефект нарушает процесс восстановление активной формы тетрагидробиоптерина, принимающего участие в виде кофактора при гидроксилировании фенилаланина в тирозин, а также предшественников нейромедиаторов серотонинового и катехоламинового ряда, таких как L-ДОФА и 5-окситриптофан.
Фенилкетонурию 3 диеторезистентную описал Кауфман в 1978 г. (согласно источнику Википедия). Она отличается недостаточностью 6-пирувоил тетрагидроптерин синтетазы, принимающей участие в синтезе тетрагидробиоптерина.
Атипичные формы отличаются прогрессированием проявлений заболевания.
Другие формы патологии связаны с нарушением иных альтернативных путей метаболизма фенилаланина с формированием метилминдальной ацидурии и парагидроскифенилуксусной ацидурии.
Причины возникновения фенилкетонурии
Благодаря накоплению опыта в области диагностики и лечения фенилкетонурии с течением времени стало понятно, что причины возникновения этого наследственного недуга кроются в мутациях гена, кодирующего фенилаланин-4-гидроксилазу — 12q23.2. Тип наследования аутосомно-рецессивный.
Чаще всего болезнь вызвана резко сниженной или полностью отсутствующей активностью такого фермента печени как фенилаланин-4-гидроксилаза, которая в норме необходима для катализации превращения (гидроксилирования) фенилаланина в аминокислоту — тирозин.
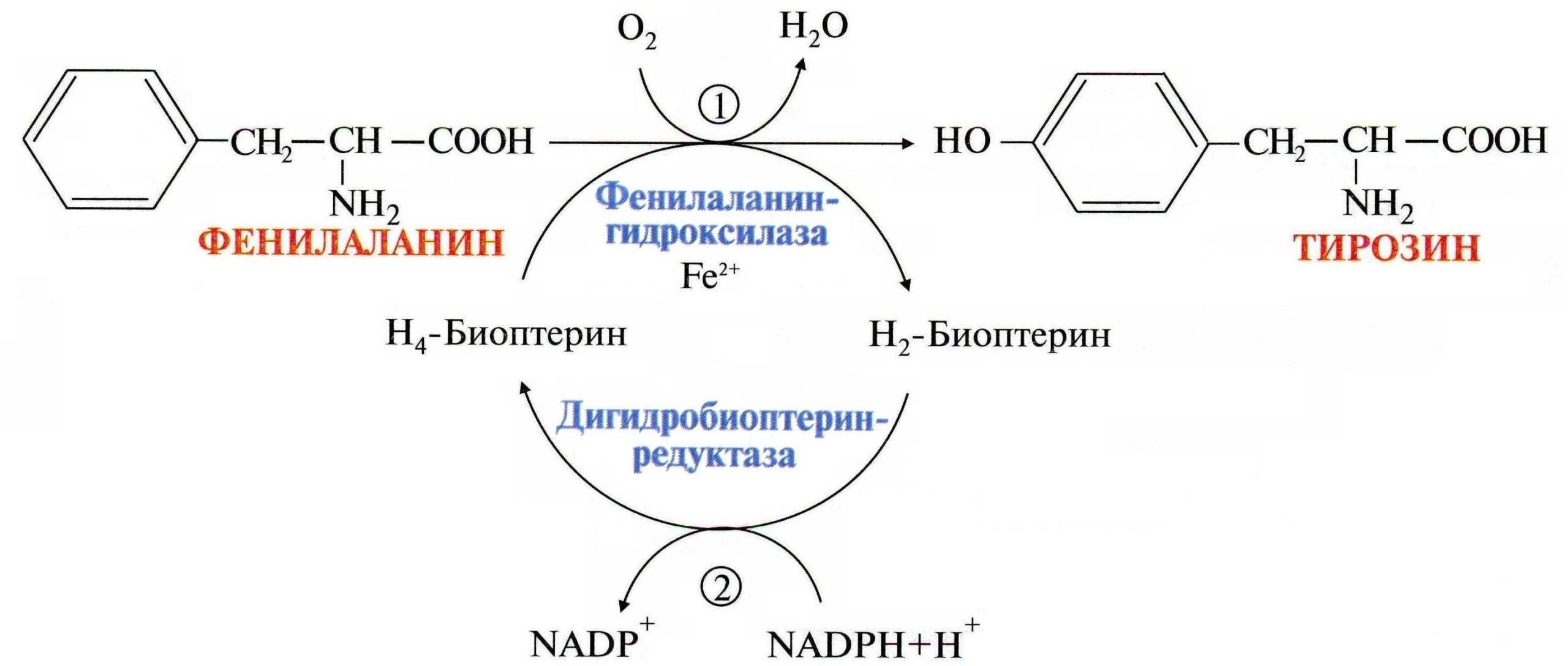
Обмен фенилаланина и тирозина
Однако, примерно в 10% случаев гиперфенилаланинемии воздействую атипичные факторы, связанные с мутациями в иных генах, кодирующих ферменты, обеспечивающие синтез кофактора фенилаланингидроксилазы, известного как тетрагидробиоптерин (BH4).
Симптомы фенилкетонурии
Фенилкетонурия отличается достаточно ярко выраженной клинической картиной, включающей такие симптомы как:
- отставание физического развития с 6 месячного возраста;
- микроцефалия;
- вегетативные дисфункции;
- повышенная возбудимость и двигательная гиперактивность;
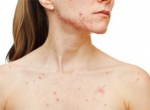
- экзема или дерматит, возможно с папулезными кожными высыпаниями (как на фото ребенка с фенилукетонурией);
- мышечная гипертензия;
- атаксия;
- гиперкинезы;
- неустойчивость походки;
- судорожные припадки;
- нередко обнаруживаются пороки сердца;
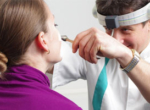
- чувствительность к травматизации и осветление кожи, волос и радужки глаз (депигментация), в особенности при несоблюдении необходимой диеты, вызывающей недостаточность меланина в организме, являющегося производным тирозина.
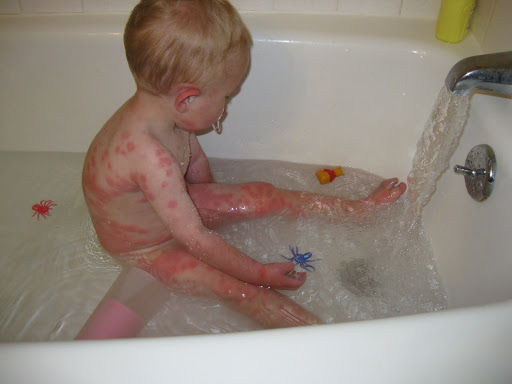
Экзема при фенилкетонурии
Психические нарушения
Фенилкетонурия вызывает значительные патологические изменения обменных процессов в головном мозге, что влечет за собой следующие нарушения:
- глубокая степень умственной отсталости, вплоть до идиотии или имбецильности;
- трудности в обучении;
- возникновение явлений эхопраксии — повторение движений за окружающими;
- эхолалии (повторение речи);
- вялое поведение может сменяться редкими вспышками злости и раздражительности.
Как можно увидеть на фото больных фенилкетонурией телосложение их обычно диспластическое, размеры черепа уменьшены, отмечается гипогенитализм и нанизм.
Анализы и диагностика
В основе диагностики фенилкетонурии лежат лабораторные анализы крови и мочи, изучают биоптаты печени, а также проводят генетические исследования:
- полуколичественный тест или количественное определение фениаланина в кровяном русле, в норме составляет 0,01-0,02 г/л, но при фенилкетонурии присутствует во всех жидких средах организма, а в сыворотке крови повышается до 0,15-0,2 г/л;
- на ранних этапах жизни (у детей 10-12 дней) могут быть выявлены в моче продукты распада фенилаланина – фенилкетоны, в особенности при нелеченой клинической картине, при этом используется проба Феллинга с 5-10% раствором FeCI3 или индикаторные бумажки «Фенистикс» и «Биофан», меняющие при положительном результате цвет на сине-зеленый;
- в печеночном биоптате исследуют уровень активности фенилаланингидроксилазы;
- проводят поиск мутаций в хромосомах гена фенилаланингидроксилазы, тогда как для 2 и 3 типа заболевания, связанного с мутациями в гене, отвечающем за биосинтез кофактора необходимо выполнение дополнительных диагностических исследований – выявления в моче низкого количества продуктов обмена нейротрансмиттеров, таких как гомованилиновая, ванилилминальная и оксииндолилуксусная кислоты.
На 3-4 сутки жизни новорожденного наиважнейшим в обнаружении обменных врождённых заболеваний оказывается неонатальный скрининг посредством анализов крови. Этот этап делает возможным обнаружить фенилкетонурию и как можно раньше начать лечение, чтобы предотвратить необратимые последствия. В РФ таким детям устанавливается категория инвалидности до 18 лет.
Лечение фенилкетонурии
Наиболее благоприятным оказывается прогноз при ранней диагностике заболевания. Если же недуг выявляется поздно, то практически невозможно справиться с уже резвившимися необратимыми изменениями тканей мозга.
В основе лечения фенилкетонурии – строгая диета, ограничивающая животные и растительные белки, которая должна длиться минимум до полового созревания, а может и пожизненно. Постоянно нужно быть в контакте с лечащим врачом, который будет мониторить состояния и психологически поддерживать пациента. При отмене диеты регулярно проводят психологические тесты, электроэнцефалограмму и определяют уровень фенилаланина в кровяном русле. Процесс ослабления диеты начинают примерно в 8-10 лет, когда заканчиваются процессы миелинизации мозга.
В случаях некоторых (мягких) форм заболевания возможно лечение кофактором (тетрагидробиоптерином) при поражённом ферменте — фенилаланингидроксилазе. Перспективными считаются разработки новых подходов лечения фенилкетонурии — использования заместительной терапии с применением фенилаланинлиазы (PAL, пегвалиазы) — растительного фермента, завершающего метаболизм фенилаланина безвредными метаболитами, а также генотерапия, в основе которой введение в организм вирусного вектора с геном фенилаланингидроксилазой. Такие методы не смогли пока выйти из стен лабораторных исследований.
При атипичных формах, не поддающихся диетотерапии, лечение сводится к введению препаратов тетрагидробиоптерина либо его синтетических аналогов, к примеру, сапроптерина.
Наиболее перспективной методикой лечения данного тяжелого заболевания является генотерапия как классический образец успешной борьбы и организационной помощи при наследственных патологиях.
Доктора
Лекарства
Медикаментозно лечение обычно симптоматическое с применением:
- аскорбиновой кислоты;
- гепатопротекторов — Эссенциале Форте, Карсила, Рибоксина и т.д.;
- нооторопов — Энцефабола, Ноотропила, Церебролизина и других;
При отсутствии эффекта от диетотерапии в случаях атипичных форм болезни проводят заместительную терапию L-ДОФА (Наком, Леводопа) и 5-гидрокситриптофаном (суточная доза — 10-20 мг/кг).
Процедуры и операции
- ЛФК;
- массаж.
Фенилкетонурия у детей
Для фенилкетонурии характерна вариабельность клинической картины. Изначально новорожденные выглядят совершенно нормально, у них отмечается хорошая прибавка в весе. Однако, в некоторых случаях с первых дней можно обнаружить вялость, сонливость, реже беспокойность, неспособность фиксации взгляда на предметах, отсутствие реакции на источник звука, позднее начинают гулить.
Возраст 2-4 месяцев характеризуется манифестацией таких симптомов у детей как:
- вялость;
- беспокойство и раздражительность;
- отсутствие интереса к окружающему миру;
- экзема и возможно — себорея;
- судороги;
- рвота и частые срыгивания, затрудняющие процесс вскармливания;
- гиперрефлексия;
- изменение запаха пота и мочи на «мышиный», называемый еще «запахом волка».
При беременности
Женщинам с фенилкетонурией, которых успешно лечили с помощью диеты, следует крайне внимательно относится к своему состоянию во время вынашивания ребенка, ведь даже при генетически нормальном развитии плода высок риск нарушений из-за повышенного уровня фенилаланина и его метаболитов в кровоток матери как серьезного тератогенного фактора с нейротропной токсичностью. Поэтому, перед зачатием таким пациенткам рекомендуют вернуться к строгой диете и придерживаться ее всю беременность.
Особая диета должна ограничивать потребление до 15-20 мг/кг фенилаланина в сутки, и при этом следить, чтобы не развивался дефицит незаменимых аминокислот.
Диета при фенилкетонурии

Безбелковая диета
- Эффективность: лечебный эффект через 2 недели
- Сроки: до достижения эффекта
- Стоимость продуктов: 1200-1300 руб. в неделю
Особам с фенилекетонурией крайне важно придерживаться строгой диеты, ограничивающей белковую пищу, включая мясо, рыбу, яйца, молокопродукты, колбасные изделия и другие продукты, содержащие животные или растительные белки. Для восполнения дефицита белков употребляют аминокислотные смеси без фенилаланина. Обычно рекомендуют такие белковые гидролизаты как Лофеналак, Фенилфри, Берлофен, Апонти, Гипофенат для детей до 4-5 лет и Нофелан – детям старше 5 лет.
В основе рациона обычно овощные и фруктовые соки, а также пюре, продукты с малым содержанием белков — саго, хлеб, макароны, крупка, приготовленная на крахмальной основе, сахар и варенье.
В некоторых современных газированных напитках, жевательных резинках и лекарственных препаратах содержится фенилаланин в виде аспартама, о чём производитель обязан предупреждать на упаковке, но они не всегда придерживаются этого правила, поэтому необходимо быть крайне осторожным при выборе продуктов. На некоторых безалкогольных напитках, к примеру, после данных о составе и пищевой ценности в 100 мл продукта выписано такое примечание: «В напитке содержится источник фенилаланина. Противопоказано в случае фенилкетонурии».
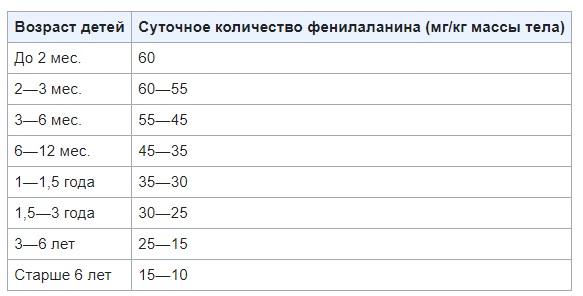
Допустимые значения фенилаланина при фенилкетонурии в разном возрасте детей
Внимание! Составлять диету для пациентов с фенилкетонурией должен квалифицированный специалист, способный учесть все потребности организма в фенилаланине и его допустимое количество потребления.
Список источников
- Ковалев В.В. Психиатрия детского возраста. Руководство для врачей. Москва: «Книга по требованию », 1979. – С. 482-487.
- Карен Маркданте, Роберт Клигман. Основы педиатрии по Нельсону. -М.: Эксмо, 2021. - С. 224-229.






 Эссенциале форте Н
Эссенциале форте Н Карсил
Карсил Рибоксин
Рибоксин Энцефабол
Энцефабол Ноотропил
Ноотропил Наком
Наком















Последние комментарии
Надежда: Наконец нашла эту статью, где рассказано как правильно питаться, после удаления желудка ...
Алла Анатольевна: Как только прочитаешь противопоказания, сразу сдохнуть хочется.
Елена: Мой опыт положительный. Я выпила эскапел, потом еще сделала тест, потом сделала узи и ...
Сергей Степанов: Занимаюсь тяжёлой атлетикой уже много лет, колени давно начали шалить. Врач посоветовал ...